 |
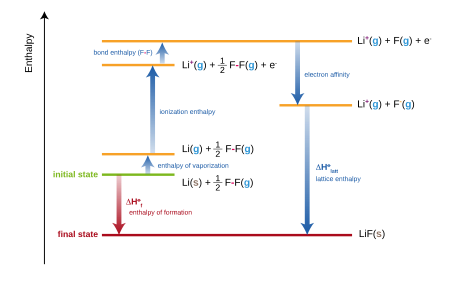
| Diagram Siklus Born-Haber Perubahan Entalpi Pembentukan Standard LiF (Sumber: wikipedia.org) |
Perhitungan Perubahan Entalpi (∆H) Reaksi Berdasarkan Data ∆Hfo
- Perubahan entalpi (∆H) suatu reaksi adalah jumlah total perubahan energi pemutusan ikatan (ruas pereaksi/ruas kiri) dengan total energi pembentukan ikatan (ruas produk/kanan)
- Secara sederhana perubahan entalpi (∆H) suatu reaksi kimia dituliskan sebagai:
∆H Reaksi = ∑∆Hfo Produk — ∑∆Hfo Pereaksi
atau
∆H Reaksi = ∑∆Hfo Ruas Kanan — ∑∆Hfo Ruas Kiri
- Unsur bebas adalah unsur yang tidak berikatan dengan unsur lain dan tidak memiliki muatan
- Berikut adalah contoh tabel data nilai ∆Hfo beberapa senyawa
 |
| Harga ∆Hfo Unsur Bebas Seperti C, H2 dan N2 Adalah Sama Dengan Nol |
Contoh:
∆Hfo CH4O (l) = —238,6 kJ/mol
∆Hfo CO2 (g) = —393,5 kJ/mol
∆Hfo H2O (l) = —286 kJ/mol
a. Tentukan ∆H reaksi pembakaran CH4O (l) sesuai reaksi:
CH4O (l) + 3/2 O2 (g) → CO2 (g) + 2H2O (l)
b. Tentukan jumlah kalor yang dibebaskan pada pembakaran 8 gram metanol (CH4O).
(Ar H = 1, C = 12 dan O = 16)
Pembahasan:
a. ∆H reaksi pembakaran CH4O (l)
| Pereaksi (Ruas Kiri) | Produk (Ruas Kanan) | ||||
| ∆Hfo (kJ/mol) | —238,6 | 0 | —393,5 | —286 | |
| Reaksi: | CH4O (l) | 3/2 O2 (g) | → | CO2 (g) | 2H2O (l) |
| Jumlah ∆Hfo (kJ) | —238,6 | 0 | —393,5 | —572 | |
| —238,6 kJ | —965,5 kJ | ||||
∆H Reaksi = ∑∆Hfo Produk — ∑∆Hfo Pereaksi
∆H Reaksi = —965,5 kJ — ( —238,6 kJ ) = —726,9 kJ
Karena koefisien reaksi metanol (CH4O) pada reaksi di atas adalah 1 (ingat, koefisien reaksi menunjukkan jumlah mol), sehingga bisa disimpulkan bahwa H reaksi pembakaran metanol adalah sebesar —726,9 kJ/mol. Tanda minus menunjukkan arti reaksi eksoterm
b. ∆H reaksi pembakaran 8 mol metanol (CH4O (l))
Dari perhitungan nomor (a) diketahui bahwa kalor pembakaran metanol adalah sebesar 726,9 kJ/mol,
Sehingga kita harus menghitung dahulu jumlah mol 8 gram metanol (CH4O).
| Massa CH4O | 8 gram |
| Mr CH4O | 32 |
| Sehingga | |
| Mol = gram/Mr | 0,25 mol |
| Kalor pembakaran 0,25 mol CH4O | 726,9 kJ/mol x 0,25 mol |
| 181,725 kJ | |
(Semoga Bermanfaat - Ahmad Fata)
Referensi
- Utami, Budi dkk, Kimia 2 : Untuk SMA/MA Kelas XI, Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional, 2009